E-Online | Elektronik Grundlagen |
Primärelement
Ein Primärelement ist ein elektrochemischer Spannungserzeuger, und wird auch Batterie genannt.
Galvanisches Element:
Beim Eintauchen eines Metalls in eine Säure findet ein Ionisierungsprozeß statt. Je nach Särekonzentration und Art des Metalls geht das Metall unterschiedlich stark in Lösung. Dabei werden Elektronen freigesetzt. Gleichzeitig entsteht eine elektrische Spannung, die je nach Metall variiert.
Batterie-Prinzip:
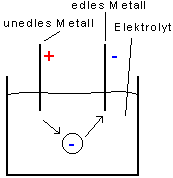 Beim Stromfluß zersetzt sich das unedle Metall. Das edle Metall nimmt dabei Elektronen auf und wird negativ. Das unedle Metall gibt Elektronen ab und wird positiv.
Beim Stromfluß zersetzt sich das unedle Metall. Das edle Metall nimmt dabei Elektronen auf und wird negativ. Das unedle Metall gibt Elektronen ab und wird positiv.
Elektrochemische Spannungsreihe (Normalpotentiale):
Metalle, die gegenüber dem Wasserstoff eine positive Spannung haben, werden edle, alle mit einer negativen Spannung werden als unedle Metalle bezeichnet.
| Metall | Potential |
|---|
| Fluor (F) | +2,85V |
| Gold (Au) | +1,50V |
| Platin (Pt) | +0,87V |
| Silber (Ag) | +0,80V |
| Kohlenstoff (C) | +0,75V |
| Kupfer (Cu) | +0,35V |
| Wasserstoff (H2) | 0V |
| Blei (Pb) | -0,13V |
| Zinn (Sn) | -0,14V |
| Nickel (Ni) | -0,25V |
| Cadmium (Cd) | -0,40V |
| Eisen (Fe) | -0,44 |
| Chrom (Cr) | -0,56V |
| Zink (Zn) | -0,76V |
| Mangan (Mn) | -1,05V |
| Aluminium (Al) | -1,66V |
| Magnesium (Mg) | -2,36V |
| Lithium (Li) | -3,02V |
Beispiel: Zink-Kohle-Element
Zink = -0,76V
Kohle = +0,75V
Daraus ergibt sich eine Differenzspannung von 1,51V.
Das Zink-Kohle-Element ist als Batterie besonders geeignet, da beide Stoffe in der Natur häufig vorkommen, und so sehr billig sind.
Werden höhere Spannungswerte aus der Tabelle ermittelt, so hat das die Folge, das höhere Materialkosten und eine kürzere Lebensdauer auftritt.
Weitere verwandte Themen:
 Beim Stromfluß zersetzt sich das unedle Metall. Das edle Metall nimmt dabei Elektronen auf und wird negativ. Das unedle Metall gibt Elektronen ab und wird positiv.
Beim Stromfluß zersetzt sich das unedle Metall. Das edle Metall nimmt dabei Elektronen auf und wird negativ. Das unedle Metall gibt Elektronen ab und wird positiv.